 Παρά το γιγαντιαίο βήμα που είχε κάνει η επιστήμη προς την κατανόηση της ραδιενέργειας (τέλη του 19ου αιώνα), οι επιστήμονες ακόμη καταλάβαιναν πολύ λίγα από τον κόσμο του ατόμου. Η αιτία ήταν, ότι τα μοντέλα του ατόμου δεν μπορούσαν να εξηγήσουν τα φαινόμενα αυτά. Όμως μερικά χρόνια αργότερα η εργασία του Νεοζηλανδού φυσικού Ernest Rutherford (1871-1937) επέτρεψε να εισέλθουν οι φυσικοί στον κόσμο του ατόμου. Σε μια μακρά και διακεκριμένη καριέρα ο Rutherford έθεσε τα θεμέλια για τον καθορισμό της ατομικής δομής της ύλης.
Παρά το γιγαντιαίο βήμα που είχε κάνει η επιστήμη προς την κατανόηση της ραδιενέργειας (τέλη του 19ου αιώνα), οι επιστήμονες ακόμη καταλάβαιναν πολύ λίγα από τον κόσμο του ατόμου. Η αιτία ήταν, ότι τα μοντέλα του ατόμου δεν μπορούσαν να εξηγήσουν τα φαινόμενα αυτά. Όμως μερικά χρόνια αργότερα η εργασία του Νεοζηλανδού φυσικού Ernest Rutherford (1871-1937) επέτρεψε να εισέλθουν οι φυσικοί στον κόσμο του ατόμου. Σε μια μακρά και διακεκριμένη καριέρα ο Rutherford έθεσε τα θεμέλια για τον καθορισμό της ατομικής δομής της ύλης.
Γύρω στο 1904 οι William Henry Bragg και Richard Daniel Kleeman, είχαν ανακαλύψει ότι σωμάτια α σταθερής ενέργειας είχαν την ίδια εμβέλεια, ενώ οι δύο Bragg (πατέρας και γιος) είχαν μελετήσει τον ιονισμό κατά μήκος της τροχιάς τους.
O Rutherford από το 1906 αντιμετώπιζε ένα μεγάλο πρόβλημα: να περιγράψει και να ερμηνεύσει τα φαινόμενα που συνόδευαν τη διέλευση των σωματίων α μέσω της ύλης. Επί μερικά χρόνια, έκανε πειράματα στα οποία εκτόξευε σωματίδια α πάνω σε λεπτά φύλλα από διάφορα υλικά, με το σκεπτικό ότι, ακόμη και αν τα σωματίδια διαπεράσουν το υλικό, μπορεί να υποστούν εκτροπή και σκέδαση από τα άτομα που το αποτελούν. Από την μορφή της εκτροπής, ήθελε να συναγάγει συμπεράσματα σχετικά με την δομή του ατόμου.
Έτσι, μαζί με τους μαθητές του Hans Geiger και Ernest Marsden, το 1908 διηύθυνε μια σειρά πειραμάτων στα οποία βομβάρδιζε ένα φύλο χρυσού με θετικά φορτισμένα σωμάτια α, που εκπέμπονταν από ραδιενεργό υλικό. Τα περισσότερα από τα σωμάτια περνούσαν ανεμπόδιστα μέσα από το φύλο, δείχνοντας ότι στο εσωτερικό του φύλου υπήρχε ένας, σχεδόν κενός χώρος, παρά μια διάταξη συμπαγών ατόμων, που όπως πίστευε ο Thomson, ήσαν διατεταγμένα πυκνά το ένα δίπλα στο άλλο. Παρόλα αυτά μερικά σωμάτια α αναπηδούσαν προς τα πίσω, υποδεικνύοντας έτσι την παρουσία και κάποιων συμπαγών μερών της ύλης πάνω στα οποία ανακλώνταν τα σωμάτια. Τα συμπαγή αυτά μέρη δημιουργούσαν ένα ισχυρό ηλεκτρικό πεδίο, αφού έκανε τα σωμάτια α να ανακλώνται.
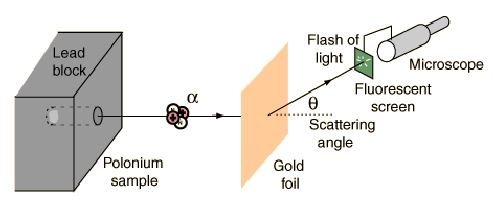
Το διάσημο πείραμα που αποκάλυψε την δομή του ατόμου
 Αριστερή πάνω εικόνα: αυτό που ανέμεναν οι Marsden – Geiger, να διέρχονται οι ακτίνες άλφα σχεδόν ανενόχλητα μέσα από το φύλο του χρυσού. Κάτω αριστερή εικόνα: ένα μικρό μέρος των ακτίνων άλφα γύριζε πίσω, σαν να είχε κτυπήσει σε τοίχο
Αριστερή πάνω εικόνα: αυτό που ανέμεναν οι Marsden – Geiger, να διέρχονται οι ακτίνες άλφα σχεδόν ανενόχλητα μέσα από το φύλο του χρυσού. Κάτω αριστερή εικόνα: ένα μικρό μέρος των ακτίνων άλφα γύριζε πίσω, σαν να είχε κτυπήσει σε τοίχο
Στο πείραμα εκτόξευε σωματίδια α πάνω σε ένα φύλλο χρυσού πάχους μόλις 1/20.000 του εκατοστού. Τα περισσότερα σωματίδια διήλθαν από το φύλλο χωρίς να εκτραπούν από την τροχιά τους και καταγράφηκαν στην φωτογραφική πλάκα που υπήρχε πίσω από αυτό.
Αφού ο χρυσός αποτελούσε ένα εμπόδιο με πάχος τουλάχιστον δύο χιλιάδων ατόμων, το γεγονός ότι τα σωματίδια α διαπερνούσαν το φύλλο σαν να μην συναντούσαν τίποτα οδηγούσε στο συμπέρασμα ότι τα άτομα αποτελούνται στο μεγαλύτερο μέρος τους από κενό χώρο. Ωστόσο, μερικά σωματίδια α υπέστησαν εκτροπή και χτύπησαν την φωτογραφική πλάκα σε ορισμένη απόσταση από το κεντρικό σημείο όπου προσέπιπτε η κύρια ροή των σωματιδίων. Σε μερικές περιπτώσεις, μάλιστα, η γωνία εκτροπής ήταν αρκετά μεγάλη.
Αυτό σήμαινε ότι ένα μέρος του ατόμου περιέχει αξιοσημείωτη μάζα. Και από το γεγονός ότι τόσο λίγα σωματίδια α παρουσίαζαν εκτροπή έβγαινε το συμπέρασμα ότι το μέρος που περιέχει την μάζα αποτελεί ένα πολύ μικρό τμήμα του ατόμου.
Οι δύο μαθητές του Ράδερφορντ παρατήρησαν λοιπόν τυχαία ότι κάποια σωμάτια άλφα αντί να κινούνται ευθύγραμμα ή περίπου ευθύγραμμα εκτρέπονταν σημαντικά από την ύλη.
Όταν ο Marsden ανέφερε ότι μερικοί πυρήνες ηλίου (σωμάτια άλφα) δεν ακολουθούσαν τον γενικό κανόνα της ευθύγραμμης πορείας, ο Ράδερφορντ του είπε να επαναλάβει το πείραμα για να την επιβεβαιώσει. H μεγάλη εκτροπή των σωματίων άλφα είχε αφήσει κατάπληκτο τον Ράδερφορντ, που αργότερα είπε ότι ήταν σαν να έριχνε κάποιος σφαίρες σ’ ένα φύλλο χαρτί κι αυτές αναπηδούσαν προς τα πίσω!
Μέχρι το 1911, ο Rutherford είχε συγκεντρώσει αρκετά δεδομένα ώστε να ανακοινώσει την θεωρία του για τον πυρήνα τον ατόμου και γιατί υφίστανται μεγάλη εκτροπή τα σωμάτια άλφα. Σύμφωνα με την θεωρία αυτή, όλη σχεδόν η μάζα του ατόμου είναι συγκεντρωμένη σε έναν μικροσκοπικό, θετικώς φορτισμένο, πυρήνα (του οποίου η διάμετρος, όπως ξέρουμε σήμερα, είναι μόλις το 1/100.000 της διαμέτρου του ατόμου). Τα εξωτερικά μέρη του ατόμου περιέχουν τόσα ηλεκτρόνια (που το καθένα φέρει μια μονάδα αρνητικού φορτίου), ώστε το φορτίο του πυρήνα να εξουδετερώνεται και το άτομο στο σύνολο του να εμφανίζεται ηλεκτρικά ουδέτερο.
Έδειξε έτσι ότι το ατομικό μοντέλο του J.J. Thomson – το μοντέλο του σταφιδόψωμου όπως ονομάστηκε – ήταν εσφαλμένο.
O Ράδερφορντ δήλωσε κατηγορηματικά ότι δεν τον ενδιέφερε το πρόβλημα της ευστάθειας του συστήματος, που ήταν και το ασθενές του σημείο και δημιουργούσε σημαντικές δυσκολίες.
Στο πλαίσιο αυτού του πλανητικού μοντέλου ο ίδιος απλώς ανέφερε ότι μια σειρά από μικροσκοπικά ηλεκτρόνια στρέφονται γύρω από τον πυρήνα, όπως η Γη γύρω από τον ήλιο, ή ένας δακτύλιος γύρω από τον Κρόνο. Ωστόσο, η συγκέντρωση της μεγαλύτερης μάζας του ατόμου σε ένα πολύ μικρό πυρήνα, έκανε το πλανητικό μοντέλο του ατόμου να μοιάζει ακόμα περισσότερο με το ηλιακό μοντέλο. Καθώς ξέρουμε ότι ο ήλιος – πυρήνας – περιέχει το μεγαλύτερο μέρος της μάζας του ηλιακού μας συστήματος.
Σύμφωνα με τη θεωρία του καθώς ένα σωμάτιο α, που θεωρείται ως φορτισμένο υλικό σημείο, προσέγγιζε τον πυρήνα, απωθείτο σύμφωνα με το νόμο του Coulomb και, όπως είχε ήδη υπολογίσει ο Νεύτωνας, ακολουθούσε μια υπερβολική τροχιά, με τον πυρήνα να θεωρείται ως ένα από τα εστιακά σημεία της υπερβολής. Τα ηλεκτρόνια, μερικές χιλιάδες φορές ελαφρότερα από τον πυρήνα, δεν επηρέαζαν την τροχιά των σωματίων α. Με το μοντέλο αυτό είναι δυνατόν να προσδιοριστεί η πιθανότητα που έχει ένα σωμάτιο α να εκτραπεί κατά γωνία θ, καθώς διέρχεται μέσα από ένα μεταλλικό έλασμα.
O Rutherford έστειλε το χειρόγραφο στο οποίο περιγράφεται η εργασία αυτή στο Philosophical Magazine, τον Απρίλιο του 1911.
Λίγο αργότερα, χρησιμοποιώντας μια απλή διάταξη οι Geiger και Marsden επιβεβαίωσαν τον μαθηματικό τύπο του μοντέλου του Ράδερφορντ σε όλες του τις λεπτομέρειες, αλλάζοντας τόσο το υλικό πάνω στο οποίο έπεφταν τα σωμάτια α, δηλαδή το Z, όσο και το πάχος του, καθώς την ταχύτητα των σωματίων α και τη γωνία θ – τη γωνία της απόκλισης της δέσμης των ακτίνων άλφα.
H θεωρία του Rutherford υιοθετήθηκε γρήγορα, γιατί έδινε απάντηση σε σημαντικά ερωτήματα. Λόγου χάρη, έγινε πια κατανοητή η σχέση ανάμεσα στα σωματίδια α και το ήλιο. Τα σωματίδια α δεν ήταν άτομα ηλίου, αλλά πυρήνες ηλίου. Αυτή η θεώρηση εξηγούσε το ηλεκτρικό φορτίο του σωματιδίου α, αλλά και την διεισδυτικότητα του, η οποία οφείλεται στο υποατομικό μέγεθος του σωματιδίου.
Ο Ernest Rutherford πήρε Νόμπελ Χημείας το 1908 για τις μελέτες του πάνω στην διάσπαση των στοιχείων καθώς και τα ραδιενεργά στοιχεία.
Δείτε όλα τα άρθρα – αφιερώματα για τις επετείους του 2011




Leave a Comment